来源:新型储能电池
研究背景
有机电极材料具有灵活的可设计性及绿色可持续性等优势,在水系锌离子电池体系中具有广阔的应用前景。然而目前有机材料面临着两个主要的挑战,即差的导电性和高的溶解度。这进一步限制了水系锌-有机电池的电化学性能。本工作设计了一种含有分子内氢键的有机聚合物(H-PNADBQ),很好的改善了以上两个问题。理论计算和实验结果表明:分子内氢键的构筑(1)降低了分子的极化和反应位点的分子静电势,从而抑制有机分子的溶解;(2)提升了有机材料的电子电导性;(3)改善了H-PNADBQ的π共轭效应,从而提升了电荷转移动力学。因此,基于富含分子内氢键的H-PNADBQ正极组装的水系锌-有机电池表现出较好的循环稳定性(负载为10 mg cm⁻²的H-PNADBQ正极在125 mA g⁻¹的电流密度下稳定循环290圈)和倍率性能(25 A g⁻¹的电流密度下的放电容量为137.1 mAh g⁻¹)。
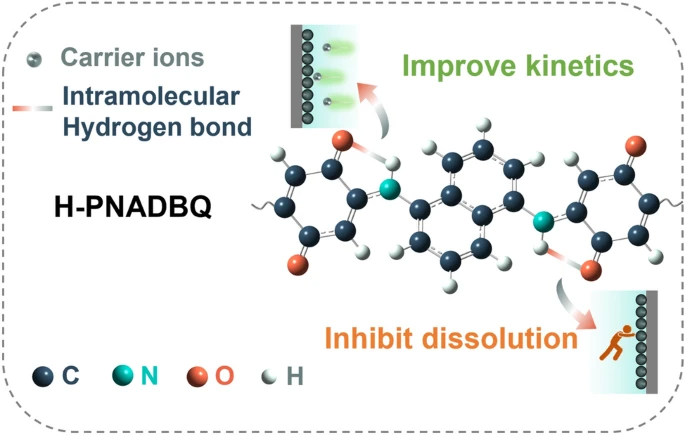
Intramolecular Hydrogen Bond Improved Durability and Kinetics for Zinc-Organic Batteries
Tianjiang Sun, Jun Pan, Weijia Zhang, Xiaodi Jiang, Min Cheng, Zhengtai Zha, Hong Jin Fan*, Zhanliang Tao*
Nano-Micro Letters (2024)16: 24
https://doi.org/10.1007/s40820-023-01263-7
本文亮点
1. 设计了具有分子内氢键的聚合物正极H-PNADBQ。验证了分子内氢键可以改善有机材料的溶解和电导率差的问题。
2. 基于分子内氢键设计,高负载的H-PNADBQ正极(5和10 mg cm⁻²)在低电流密度下表现出较好的循环稳定性。
内容简介
对于发展高性能的水系锌离子电池而言,正极材料尤为重要。相比于无机正极材料,有机材料具有灵活的结构可设计性及电化学性质可调性,且基于表面官能团的协同反应机制使得有机材料理论上表现出较快的反应动力学。然而,有机材料通常面临着高的溶解度和低的电导率。基于这两个问题,南开大学陶占良教授&南洋理工大学范红金课题组提出构筑分子内氢键策略来抑制有机材料的溶解和改善其电子电导性。理论研究和实验结果表明,分子内氢键不仅可以通过降低反应活性位点的静电势和分子的极化来降低分子在水系电解液中的溶解度,还可以通过提升分子的π共轭效应来促进电荷转移从而加速其反应动力学。
图文导读
I 富含分子内氢键的H-PNADBQ聚合物的合成及表征
以苯醌和1,5-萘二胺为原料通过简单温和的聚合反应合成了富含分子内氢键的有机聚合物H-PNADBQ。该聚合物表现出球形形貌,直径大约2~3微米,这增大了其与电解液的接触面积。通过TEM-mapping图可以看出C, N ,O元素的均匀分布。通过红外光谱可以看到,在高波数可以明显观察到两种化学环境的N-H伸缩振动峰,即自由的N-H伸缩振动及形成分子内氢键的N-H···O伸缩振动峰。
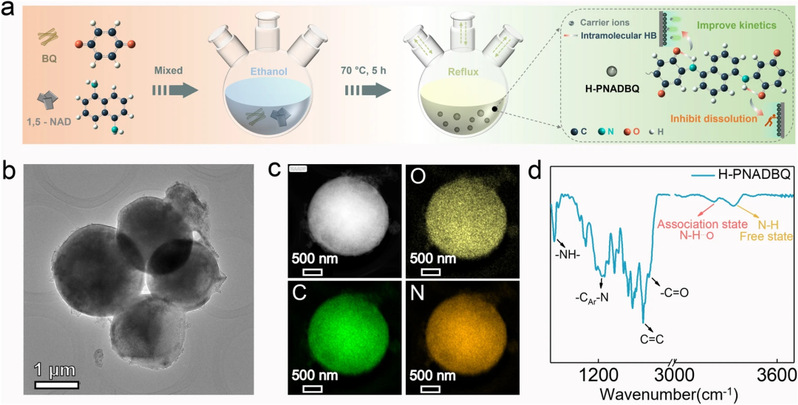
图1. H-PNADBQ聚合物的(a)合成步骤及作用机制;(b)TEM; (c)TEM-Mapping;以及(d)红外光谱。
II H-PNADBQ的理论研究和光电子能测试
我们搭建了不含有分子内氢键的聚合物模型PNADBQ作为对照组,以此来研究分子内氢键的性质及作用。可以看到,优化后的H-PNADBQ分子中,氢键的键长为2.15 Å,键能为0.45 eV,这与基于Atoms-in-molecules theory计算的结果较为吻合(0.42 eV)。H-PNADBQ的溶解自由能高于PNADBQ,表明分子内氢键可以抑制材料的溶解。另外,形成分子内氢键后,H-PNADBQ的C=O反应为点的分子静电势值降低,从而降低了分子的亲水性,这可以降低材料的溶解度。图(d)可以看出相比于PNADBQ,H-PNADBQ的四个环的多中心键级均为正值,表明形成分子内氢键后,H-PNADBQ的π共轭效应显著提升,这理论上提升电荷转移动力学。相比于苯醌,H-PNADBQ的LUMO-HOMO能级差降低,光电子能差也显著降低,这表明,形成分子内氢键后,材料的电子电导性显著提升。
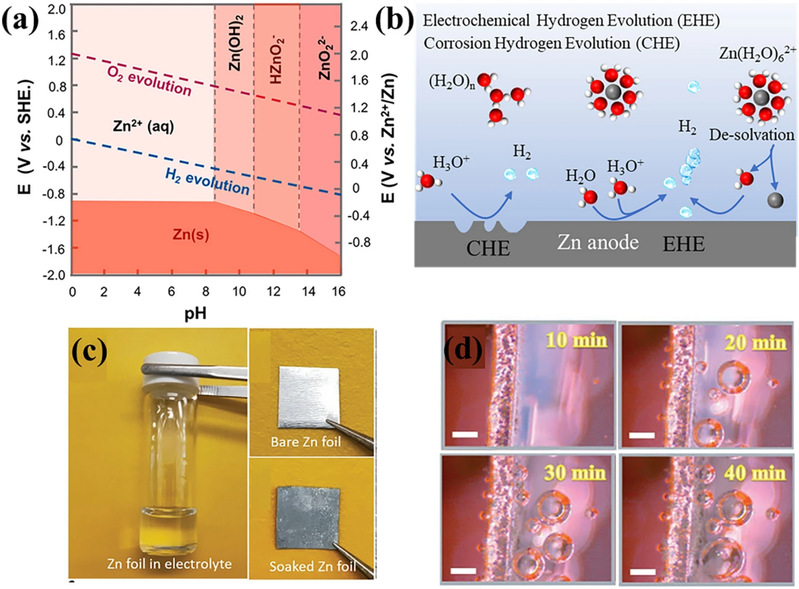
图2. (a)形成分子内氢键的相对能量;(b)PNADBQ和H-PNADBQ的溶解自由能;(c)不同分子的活性位点的分子静电势极值;(d) PNADBQ和H-PNADBQ的多中心键级及pi轨道分布;(e, f) BQ和H-PNADBQ的分子轨道能级(e)和光电子能(f)。
III Zn//H-PNADBQ电池的电化学性能测试
以2 M Zn(CF₃SO₃)₂为电解液组装的Zn//H-PNADBQ全电池表现出较好的电化学性能。在低负载下循环5000圈(5 A g⁻¹)和10000圈 (10 A g⁻¹)容量没有衰减。在高负载(5和10 mg cm⁻²),小电流密度(125 mA g⁻¹)下,循环超过290圈,容量衰减不明显。另外,H-PNADBQ也表现出较好的倍率容量。这得益于分子内氢键的构筑。
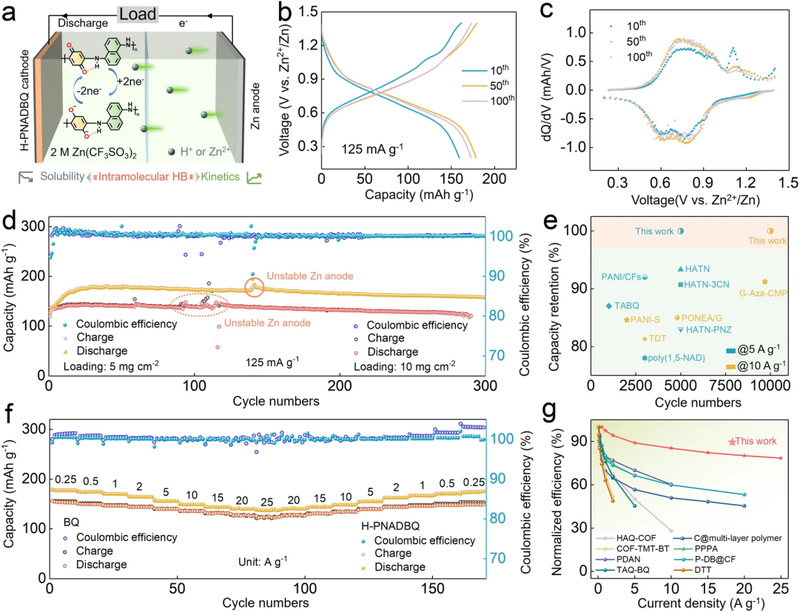
图3. Zn//H-PNADBQ电池的(a) 示意图;(b) 充放电曲线;(c) dQ/dV 曲线;(d)不同负载的长循环性能;(e)长循环性能对比图;(f)倍率性能;(g)倍率性能对比图。
IV H-PNADBQ正极的动力学及反应机理研究
既然H-PNADBQ具有较高的赝电容行为和扩散系数,组装的Zn//H-PNADBQ全电池就应该有不错的倍率性能。非原位红外谱图表明,H-PNADBQ的反应活性位点为C=O,而N-H官能团并未发生变化。放电过程可以看到C-OH和O-Zn信号的出现,并在充电过程中消失,表明H⁺/Zn²⁺的共同储存机制。另外,充电放电过程还伴随着C-F和S=O键的形成和消失,这对应于碱式副产物的生成和消失。这也可以从非原位XRD谱图及SEM图中得到验证。碱式副产物的生成通常也被认为是材料嵌入质子的证据之一。另外,通过TEM-Mapping图中发现,在放电态的活性材料中检测到Zn元素,进一步证实其Zn²⁺的储存行为。因此,作者认为,H-PNADBQ表现出H⁺/Zn²⁺的共同储存行为。
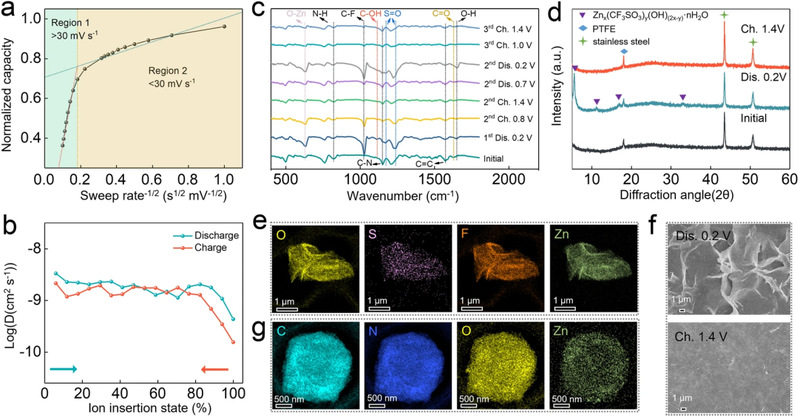
图4. (a) 动力学测试;(b)离子扩散系数;(c)非原位红外,(d)非原位XRD谱图;(e)放电态的TEM-Mapping图;(f)非原位的SEM图。